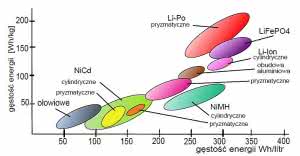
Na przykład, akumulatory ołowiowe maja bardzo małą gęstość magazynowanej energii, poniżej 50 watogodzin na kilogram. Są za to bardzo tanie i mogą oddawać stosunkowo duże prądy. Akumulatory litowe na odwrót: zapewniają uzyskanie największej gęstości energii, ale jak na razie są drogie.
Rysunek 1 pokazuje gęstość energii najpopularniejszych grup akumulatorów w watogodzinach na kilogram oraz objętościową w watogodzinach na litr. Trzeba podkreślić, że tylko najlepsze współczesne akumulatory litowe oferują gęstość energii na poziomie 200 Wh/kg.
Inne akumulatory
Oprócz tych akumulatorów istnieją też inne. Niektóre były dawniej wykorzystywane, a obecnie straciły swoje znaczenie. Inne to dopiero konstrukcje eksperymentalne, testowane i udoskonalane. Jeszcze inne są na rynku, ale ich popularność jest niewielka. Takim przykładem są...
Ładowalne alkaliczne akumulatory manganowe (RAM - Rechargeable Alkaline Manganese) to odmiana 1,5-woltowych jednorazowych ogniw alkalicznych - fotografia 2. Można je ładować kilkanaście do kilkudziesięciu razy, a czym są mniej rozładowane przed ładowaniem, tym mają dłuższą żywotność. Wykazują małe samorozładowanie, ale mają znaczną rezystancję wewnętrzną, jak jednorazowe baterie alkaliczne i choćby tylko dlatego nie można ich ładować w ładowarkach, przeznaczonych dla NiMH czy NiCd. Pomimo atrakcyjnych parametrów i cen nie upowszechniły się na rynku.
W handlu są dostępne wspomniane wcześniej akumulatory NiZn (fotografia 3).
Oprócz akumulatorów NiFe i NiZn, trzeba wspomnieć o akumulatorach srebrowo-kadmowych (AgCd) oraz o srebrowo- cynkowych ( AgZn, gdzie substancjami czynnymi elektrod są Zn, ZnO, Ag2O, a elektrolitem wodny roztwór KOH. Od dawna w nielicznych zastosowaniach wykorzystywano klasyczne mokre akumulatory AgZn (np. www.greencisco.com/en/Product-68.html), a obecnie dostępne są mniejsze wersje, jak na fotografii 4 ( http://zpowerbattery.com).
Natomiast tak zwane akumulatory srebrowo-wapniowe, oferowane do samochodów, są w rzeczywistości akumulatorami kwasowo-ołowiowymi z dodatkiem srebra i wapnia.
W ostatnich latach przedstawiono szereg interesujących konstrukcji eksperymentalnych. Należą do nich akumulatory cynkowo-powietrzne (Zn-Air, Zn-Luft). Od dawna znane są jednorazowe ogniwa cynkowo-powietrzne, powszechnie wykorzystywane w aparatach słuchowych.
Po przezwyciężeniu szeregu trudności opracowano w tej technologii także akumulatory. Eksperymenty pokazują, że gęstość energii przekroczy w nich 400 Wh/kg, czyli dwa razy więcej niż w litowych.
Jeszcze większe nadzieje budzą akumulatory aluminiowo-powietrzne, ale informacje na ich temat są bardzo skąpe. Podobnie niewiele wiadomo o bateriach i akumulatorach litowo-powietrznych. Jak na razie eksperymenty wskazują na gęstość energii rzędu kilkuset Wh/kg, ale teoretyczna gęstość takich źródeł wynosi 11140 Wh/kg, czyli praktycznie jest równa gęstości energii benzyny (około 13000 Wh/kg).
Nadzieje budzą akumulatory niklowo-litowe (Ni-Li), które łączą zalety akumulatorów niklowych i litowo-jonowych. Spodziewana gęstość energii ma przekroczyć 900 Wh/kg, jednak jak na razie trudno rozwiązać problemy technologiczne związane z własnościami elektrolitu, a właściwie dwóch elektrolitów.
Mówi się też o akumulatorach sodowo-jonowych (Na-Ion), podobnych do litowo-jonowych, ale o spodziewanej gęstości energii rzędu 400 Wh/kg. Nośnikami prądu są tam jony sodu, w sód jest wielokrotnie tańszy i popularniejszy od litu, więc w perspektywie oznacza to niskie ceny. Opatentowano też akumulatory potasowo-jonowe (K-Ion). Nadzieję budzą też akumulatory litowo-siarkowe (LiS) o gęstości energii rzędu 500 Wh/kg, teoretycznie nawet do 2600 Wh/kg.
Jeżeli mowa o wykorzystaniu sodu, to od dłuższego czasu znane są akumulatory sodowo-siarkowe (NaS), gdzie metaliczny sód i siarka zostają stopione. Takie akumulatory mają temperaturę pracy rzędu 300...350 stopni i wykorzystywane są wyłącznie w energetyce w dużych systemach bezprzerwowego zasilania - przykład na fotografii 5 (www.nypa.gov).
Podobnie w wysokiej temperaturze pracują akumulatory sodowo-niklowe, gdzie stopiony elektrolit (Na-NiCl2) ma temperaturę 245 stopni. To też są akumulatory o potężnej pojemności i dużych rozmiarach.
Potężne możliwości mają też akumulatory wanadowe. Zostały wynalezione około roku 1985 na Uniwersytecie Nowej Południowej Walii w Australii. Około roku 2000 pojawiły się na światowym rynku pierwsze propozycje komercyjne. Koncepcja jest zupełnie inna, niż w klasycznych akumulatorach: akumulatory wanadowe to akumulatory przepływowe, często oznaczane angielskim skrótem RFB (Redox Flow Battery).
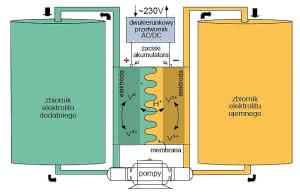
Energia jest tam magazynowana w postaci chemicznej w dużej ilości elektrolitu. Jednak w samym ogniwie znajduje się jedynie znikoma część elektrolitu. Ilustruje to w uproszczeniu rysunek 6. Dwie komory ogniwa oddzielone są półprzepuszczalną membraną. Zazwyczaj elektrody są grafitowe, komory są wyłożone grafitem, a ich wnętrze jest wypełnione watą grafitową. Przez takie przewodzące komory w obiegu zamkniętym przepompowywany jest elektrolit, pochodzący z oddzielnych zbiorników.
Membrana nie pozwala na zmieszanie obu elektrolitów, ale przepuszcza elektrony i jony wodorowe H+ (protony). W akumulatorach wanadowych elektrolitem jest kwas siarkowy z solami wanadu (siarczanem wanadylu - VO(SO4). Wanad ma tę zaletę, że występuje w pięciu stopniach utleniania i jego związki w roztworze kwasu siarkowego mogą być zarówno elektrolitem dodatnim, jak też ujemnym. Ładowanie i rozładowywanie akumulatora to po prostu zmiana stopnia utleniania metalu (wanadu), co wiąże się z pobraniem lub oddaniem elektronów.
Jedną z zalet akumulatorów przepływowych jest to, że ich pojemność nie zależy od wielkości ogniwa, tylko od ilości elektrolitu, zgromadzonego w oddzielnych zbiornikach. Natomiast wielkość ogniwa - reaktora decyduje tylko, jaką chwilową moc będzie mieć akumulator, to znaczy z jakimi prądami może pracować.
Rozładowany akumulator można naładować prądem, ale można też wymienić elektrolity na "naładowane". Taka możliwość natychmiast przywodzi na myśl zastosowanie w samochodach elektrycznych i "tankowanie" polegające na wymianie elektrolitu na "naładowany".
Idea kusząca, jednak dostępne akumulatory wanadowe, oprócz istotnych zalet, ale też dość poważne wady. Po pierwsze gęstość energii jest niska, rzędu 20...25 Wh/kg, czyli niższa niż w akumulatorach kwasowych. Wąski jest też użyteczny zakres temperatur pracy, zdecydowanie za mały jak na zastosowania motoryzacyjne. Niemniej trwają prace nad poprawą parametrów.
Akumulatory wanadowe próbowano wykorzystać w wózkach golfowych. Ale generalnie akumulatory przepływowe nie zdobyły szerszej popularności. Nie są dostępne małe akumulatory wanadowe. Ekonomiczny sens mają tylko duże instalacje do gromadzenia dużych ilości energii, na przykład na farmach wiatrowych czy w dużych instalacjach solarnych.
Ich moc sięga kilku megawatów, a pojemności wynoszą od 100000 Ah do 10000000 Ah. Takie akumulatory wanadowe zawierają tysiące litrów kwasu siarkowego. Dla porównania, akumulator samochodowy 12 V 50 Ah gromadzi 0,6 kWh energii, więc akumulator wanadowy o pojemności 6 MWh jest odpowiednikiem 10 tysięcy przeciętnych akumulatorów samochodowych.
Znane są też inne rodzaje akumulatorów przepływowych, m.in. żelazowo-chromowe czy cynkowo-bromowe - przykład na fotografii 7 (http://redflow.com).
Według Wikipedii (http://en.wikipedia.org/wiki/Flow_battery) akumulator przepływowy wykorzystujący wodór i chloran litu może osiągnąć gęstość energii 1400 Wh/kg.
A jeżeli mowa o przepływowych akumulatorach wodorowych, czy też akumulatorach protonowych (jon wodoru to proton), koniecznie trzeba wspomnieć o ogniwach paliwowych.
Ogniwa paliwowe
Klasyczne ogniwo paliwowe zachowuje się jak bateria. Ma dwa bieguny i jest źródłem prądu stałego. Wytwarza energię elektryczną wskutek łączenia wodoru z tlenem. I ten wodór trzeba dostarczyć z zewnątrz jako paliwo. Klasyczne ogniwo paliwowe nie jest rodzajem akumulatora, ponieważ nie może być naładowane prądem elektrycznym.
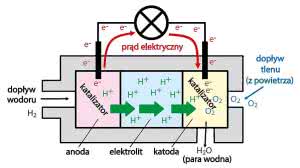
Rysunek 8 pokazuje w uproszczeniu zasadę działania. Pod wpływem katalizatora atomy wodoru rozszczepiają się na proton (H+) i elektron (e-). Protony przechodzą przez elektrolit i membranę oddzielającą elektrody wewnątrz ogniwa. Elektrony nie mogą przejść przez tę membranę i płyną od anody do katody na zewnątrz ogniwa. Jest to prąd elektryczny, który można wykorzystać. Na katodzie wodór łączy się z tlenem z powietrza i produktem reakcji jest woda (para wodna) i ciepło.
Znane są różne rodzaje ogniw paliwowych, na przykład z kwasem fosforowym (Phosphoric Acid), z membraną protonową (PEM - Proton Exchange Membrane), ze stopionym węglanem (Molten Carbonate), z tlenkiem (Solid Oxide Fuel Cells), alkaliczne, bezpośrednio wykorzystujące metanol (Direct Methanol Fuel Cells), czy regeneracyjne (Regenerative Fuel Cells). Mają odmienną budowę, pracują w różnych temperaturach i mają różną sprawność. Wiele informacji można znaleźć na stronie: www.fuelcells.org.
Ogniwa paliwowe, będące odmianą baterii nie są nowym wynalazkiem. Pierwsze takie ogniwo William Grove zbudował w Anglii już w roku 1839, czyli wcześniej, niż powstał akumulator ołowiowy. Jednak dopiero w latach 50. i 60. XX wieku zainteresowano się nimi poważniej, a to w związku z potrzebami przemysłu kosmicznego.
Dziś szereg firm produkuje wielkie ogniwa paliwowe, dostarczające setek kilowatów, a nawet kilku megawatów energii, mogące służyć jako źródła awaryjnego zasilania dla budynków, a nawet osiedli.
Podejmuje się próby wykorzystania ogniw paliwowych do napędu samochodów. Wiele uwagi poświęca się też miniaturowym ogniwom paliwowym, które w przyszłości będą zasilać przenośne urządzenia elektroniczne, na przykład komputery, telefony komórkowe, kamery wideo, konsole do gier, itd.
We wszystkich ogniwach paliwowych ostatecznie paliwem jest zawsze dostarczany z zewnątrz wodór (także zawarty w różnych substancjach, np. w metanie, metanolu, etanolu, węglowodorach, biogazie, itp). Teoretyczna sprawność ogniw paliwowych może sięgnąć 30000 Wh/kg, czyli około trzykrotnie więcej niż benzyny.
Od lat prowadzone są też eksperymenty, by uzyskać odwracalne ogniwo paliwowe, czyli akumulator wodorowy (akumulator protonowy). W praktyce dużym problemem okazuje się wtedy zapewnienie dużej sprawności zarówno ładowania, jak i rozładowania oraz magazynowanie wodoru powstającego podczas ładowania.
Tu od razu przypominają się akumulatory niklowo-metalowo-wodorkowe (NiMH), gdzie wodór wiązany jest w stopie metali tworząc wodorki metali. Pomysł jest, nie tylko zresztą ten jeden, eksperymenty trwają, jednak jak na razie, nie ma odwracalnych ogniw paliwowych, które mogą być użytecznymi akumulatorami. Niemniej perspektywy także w tym zakresie są obiecujące.
A jeżeli w omawianiu akumulatorów doszliśmy do ogniw paliwowych, to musimy też wspomnieć o superkondensatorach.
Super(ultra)kondensatory
Klasyczne kondensatory mają małą pojemność, więc ilość magazynowanej energii (E = 0,5CU2) jest niewielka. Superkondensatory, zwane też ultrakondensatorami, nie mają klasycznego dielektryka, a ich działanie ściśle wiąże się ze znanym ze szkolnych lekcji zjawiskiem elektrolizy. Otóż kwasy, wodorotlenki i sole po rozpuszczeniu w wodzie ulegają dysocjacji, czyli rozpadowi na jony. Tworzą elektrolit - ciecz przewodzącą prąd elektryczny. Przykładowo w wodnym roztworze kwasu siarkowego (H2SO4) następuje dysocjacja i w powstałym elektrolicie mamy dodatnie jony wodorowe (H+) oraz ujemne jony siarczanowe (SO42-). Jony obdarzone są ładunkiem elektrycznym i mogą się przemieszczać - są więc nośnikami prądu elektrycznego.
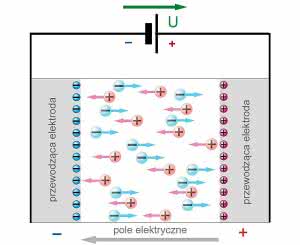
Jeżeli w elektrolicie zanurzymy dwie elektrody i dołączymy do nich źródło napięcia, to na ruchome jony zawarte w elektrolicie będą działać siły. Ładunki elektryczne o przeciwnych znakach będą się przyciągać, a ładunki jednoimienne - odpychać. Sytuacja jest przedstawiona na rysunku 9.
Do elektrody naładowanej dodatnio zdążają jony naładowane ujemnie (aniony), a do elektrody ujemnej zdążają jony dodatnie (kationy). Jeżeli dołączone napięcie U jest odpowiednio duże, to prąd będzie płynął w sposób ciągły. Jony po dotarciu do elektrod oddają lub przyjmują ładunek, wskutek czego zamieniają się w obojętne pierwiastki lub związki chemiczne, które to w postaci gazowej lub stałej wydzielają się na powierzchni elektrod.
W szkolnych doświadczeniach przeprowadza się zwykle elektrolizę wody (H2O), gdzie przepływ prądu elektrycznego powoduje wydzielanie na elektrodach tlenu (H2) i wodoru (O2). Tak jest w sytuacji, gdy napięcie dołączone do elektrod jest odpowiednio wysokie - wtedy przez elektrolit ciągle płynie prąd, a na elektrodach wydzielają się obojętne elektrycznie związki chemiczne.
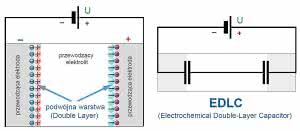
Rysunek 10. Zasada działania tzw. podwójnej warstwy izolacyjnej (Electrochemical Double-Layer Capacitor)
Inaczej jest, gdy dołączone napięcie jest małe. Już ponad sto pięćdziesiąt lat temu Hermann von Helmholtz stwierdził, że zależnie od materiału elektrody i składu elektrolitu, istnieje pewne minimalne napięcie graniczne U, potrzebne do rozpoczęcia elektrolizy.
Przy niższym napięciu elektroliza nie następuje, a elektrolit zachowuje się jak izolator. Jony gromadzą się na powierzchni elektrod, jednak nie następuje wymiana ładunków elektrycznych. Na powierzchni elektrody pojawia się tak zwana warstwa podwójna (double layer) i swego rodzaju bariera, która nie pozwala różnoimiennym ładunkom się połączyć. W efekcie układ zachowuje się tak samo jak kondensator, a właściwie jak dwa szeregowo połączone kondensatory według rysunku 10.
Taki klasyczny superkondensator składa się z dwóch podwójnych warstw. Właśnie dlatego elementy takie są nazywane EDLC (Electrochemical Double-Layer Capacitor) - kondensatorami podwójnej warstwy (z podwójną warstwą). Taka sytuacja ma miejsce tylko przy małych napięciach. Współczesne superkondensatory EDLC tego rodzaju mają napięcie nominalne najczęściej 2,7 V, a niektóre tylko około 1 V. Większe napięcie "przebija kondensatory", płynie ciągły prąd, następuje elektroliza i wydzielenie gazów, co doprowadza do rozszczelnienia obudowy.
Co istotne, podczas ładowania klasycznego kondensatora i superkondensatora EDLC nie zachodzą żadne przemiany chemiczne i można powiedzieć, że energia magazynowana jest w polu elektrycznym. Mówiąc obrazowo, potrzeba energii, żeby przemieścić jony według rysunku 9 i żeby uporządkować je i ustawić według rysunku 10. Aby je uporządkować trzeba dostarczyć energii, a potem, gdy sytuacja wraca do nieuporządkowanego stanu wyjściowego, kondensator staje się źródłem energii.
Inaczej jest w akumulatorach. Podstawą działania każdego akumulatora są reakcje chemiczne. Podczas ładowania, energia elektryczna zamieniana jest w energię chemiczną (energię wiązań chemicznych). Podczas rozładowania energia chemiczna zamienia się w energię elektryczną. Związane jest to z chemicznymi reakcjami redukcji (reduction) i utleniania (oxidation), stąd bierze się skrót redox.
Przykładowo w popularnych akumulatorach kwasowo-ołowiowych elektrolitem jest zdysocjowany roztwór kwasu siarkowego (H2SO4). Podczas rozładowania, na anodzie metaliczny ołów utlenia się do jonów ołowiu (Pb2+), które tworzą z ujemnymi jonami siarczanowymi (SO42-) nierozpuszczalny siarczan ołowiu (PbSO4) w reakcji utleniania Pb + SO42- = PbSO4 + 2e
Jednocześnie na katodzie ołów, zawarty w tlenku ołowiu, ulega redukcji do jonów ołowiu (Pb2+), które także tworzą z jonami siarczanowymi (SO42-) nierozpuszczalny siarczan ołowiu (PbSO4) w reakcji redukcji PbO2 + 4H+ + SO42- +2e = PbSO4 + 2H2O
Dlatego w miarę rozładowywania akumulatora, elektrolit zawiera coraz mniej kwasu i coraz więcej wody, co zresztą jest niezawodnym wskaźnikiem stopnia rozładowania. Podczas ładowania reakcje utleniania i redukcji przebiegają odwrotnie. Podstawy są jasne: w akumulatorach i bateriach jednorazowych energia jest magazynowana w wiązaniach chemicznych, a praca akumulatora opiera się na chemicznych reakcjach redukcji i utleniania (redox).
Historycznie biorąc, superkondensatory to kondensatory z podwójną warstwą (EDLC), jednak pojawiły się też opracowania, które też bywają nazywane superkondensatorami, ale do magazynowania energii wykorzystują reakcje chemiczne. Nazywane są też pseudokondensatorami, kondensatorami redox, a czasem kondensatorami faradajowskimi.
Trudno w przystępny sposób przedstawić szczegóły ich działania osobom mało zorientowanym w meandrach chemii i fizyki, ponieważ wykorzystane są tam specyficzne zjawiska, takie jak adsorpcja, której nie należy mylić z absorpcją. Pokrewna absorpcja to wnikanie, pochłanianie, natomiast adsorpcja to ogólnie biorąc proces wiązania się cząsteczek, atomów lub jonów na powierzchni lub na granicy faz.
I właśnie na granicy faz, między elektrodą i elektrolitem wskutek adsorpcji może tworzyć się nie tylko podwójna warstwa ładunku (double layer), ale jednocześnie mogą tam zachodzić powierzchniowe reakcje chemiczne redukcji i utleniania (redox), zwane też reakcjami faradajowskimi. Choć jednostka pojemności, farad, pochodzi od nazwiska Faraday'a, reakcje faradajowskie nie mają związku z elektrostatyczną pojemnością kondensatorów, tylko z przemianami chemicznymi.
Reakcje faradajowskie to reakcje chemiczne, podobne jak występujące w bateriach i akumulatorach, tylko występują na powierzchni elektrod, na granicy faz. Reakcje te po pierwsze związane są z przepływem tak zwanego prądu faradajowskiego, który jest wynikiem reakcji chemicznych, a nie rozdzielania ładunków, jak to ma miejsce w klasycznych kondensatorach i EDLC. Po drugie, omawiane teraz reakcje zachodzą na powierzchni, więc można się spodziewać, że będą zachodzić szybciej, niż podobne reakcje zachodzące w objętości elektrod.
Układ odpowiednio dobranej elektrody i elektrolitu zachowuje się jak kondensator, bo jest szybki, natomiast opiera się na reakcjach redox. Otrzymujemy pseudokondensator, łączący zalety kondensatorów (szybkość) i akumulatorów (duże ilości magazynowanej energii).
Zasada budowy pseudokondensatorów jest podobna, jak superkondensatorów EDLC - też potrzebna jest bardzo rozwinięta, duża powierzchnia, na której będą zachodzić adsorpcja i powierzchniowe reakcje redox.
Perspektywy są obiecujące, bowiem przy tej samej powierzchni elektrody, faradajowskie reakcje redox związane z pseudopojemnością, mogłyby dać pojemność nawet wielokrotnie większą, niż zjawisko podwójnych warstw (EDLC). Już teraz są dostępne na rynku - fotografia 11 pokazuje pseudokondensatory koreańskiej firmy Nesscap.
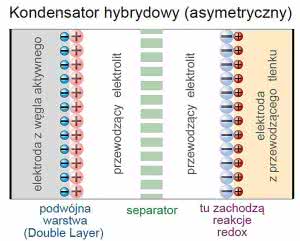
Pokrewnym rodzajem są kondensatory hybrydowe. Wykorzystują one zarówno pojemność podwójnej warstwy (EDLC), jak też pseudopojemność redox. Może to być zrealizowane albo w tej samej strukturze przez dobór odpowiednich materiałów elektrody i elektrolitu. Wtedy element taki w tej samej strukturze wykorzystuje oba zjawiska: tworzenia warstwy podwójnej (DL) i pseudopojemności redox.
Realizowane są też kondensatory hybrydowe, gdzie tylko elektrolit jest wspólny, natomiast elektrody są różne, jak pokazuje rysunek 12. Na jednej zachodzi tworzenie podwójnej warstwy (EDLC), na drugiej - reakcje faradajowskie redox.
Bywają też nazywane kondensatorami asymetrycznymi. Firma IOXUS (www.ioxus.com), oprócz ultrakondensatorów EDLC, produkuje też kondensatory hybrydowe (fotografia 13) które są kombinacją superkondensatorów i akumulatorów litowych i które dzięki pseudopojemności gromadzą do 115% więcej energii, niż klasyczne EDLC.
Ze szkolnego wzoru E = 0,5CU2 łatwo wyliczyć, że przy pojemności tysięcy faradów i napięciu rzędu 2,5...2,7V ilość magazynowanej energii jest znacząca. Gęstość energii wyrażona w Wh/kg jest wprawdzie mizerna, ale za to superkondensatory mają bardzo małą rezystancję wewnętrzną i mogą pracować przy ogromnych prądach ładowania i rozładowania, wielokrotnie większych, niż w jakichkolwiek akumulatorach.
Czyli dysponują ogromna mocą chwilową. Można je bardzo szybko ładować i rozładowywać, dlatego są stosowane m.in. w pojazdach elektrycznych, także w autobusach , a nawet lokomotywach. Pełnią tam rolę akumulatorów pomocniczych, wspomagających procesy przyspieszania i odzyskiwania energii przy hamowaniu.
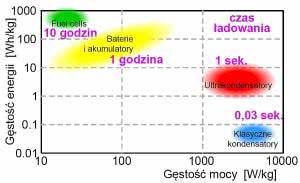
Jedną z głównych zalet superkondensatorów jest duża gęstość mocy, wyrażana w watach na kilogram, co w praktyce w praktyce możliwość pracy z ogromnymi prądami, a więc bardzo szybkie ładowanie i rozładowanie.
Za to ich gęstość energii, wyrażana w watogodzinach na kilogram, jest gorsza nawet od najgorszych akumulatorów ołowiowych. Ilustruje to rysunek 14. Z ogniwami paliwowymi jest odwrotnie: gęstość energii jest lepsza od najlepszych akumulatorów, natomiast gęstość mocy jest gorsza od najgorszych akumulatorów. Odwracalnych ogniw paliwowych, gdy powstaną, nie będzie można szybko naładować.
Oprócz przedstawionych różnych odwracalnych źródeł energii elektrycznej, wciąż prezentowane są jeszcze inne koncepcje i rozwiązania. Słyszy się o akumulatorach cienkowarstwowych, polimerowych, grafenowych...
Chodzi jednak tylko o oryginalne koncepcje, a najwyżej laboratoryjne prototypy. Jak na razie, nie widać nowej technologii, która w najbliższych latach mogłaby zagrozić aktualnie najlepszym akumulatorom litowo-jonowym. Brak akumulatorów o zdecydowanie większej gęstości energii jest też kluczową przeszkodą w upowszechnianiu się samochodów elektrycznych i hybrydowych. Niemniej dalsze perspektywy są obiecujące i warto na bieżąco śledzić postępy w dziedzinie akumulatorów.
Piotr Górecki
piotr.gorecki@elportal.pl

 Zaloguj
Zaloguj